Recent Posts
Get in touch!
Fusce varius, dolor tempor interdum tristiquei bibendum service life.
- +32 3 689 85 38
- Technology Lane 82, 9052 Ghent Belgium
- info@gulliverbiomed.com
Fusce varius, dolor tempor interdum tristiquei bibendum service life.
我們提供高品質的客製化駱駝類單域抗體(sdAbs,亦稱 VHHs 或奈米抗體)。我們擁有超過 25 年奈米抗體研發的專業經驗,能將其廣泛應用於各種生物與臨床領域。我們也提供自行開發的奈米抗體。

奈米抗體不會面臨上述問題。
駱駝類的重鏈抗體 (HcAbs) 最早於比利時布魯塞爾被發現(如下圖所示)。這類 HcAb 的抗原結合片段被稱為奈米抗體、VHH 或單域抗體。比利時是學術界與民間企業進行奈米抗體研究的重鎮。
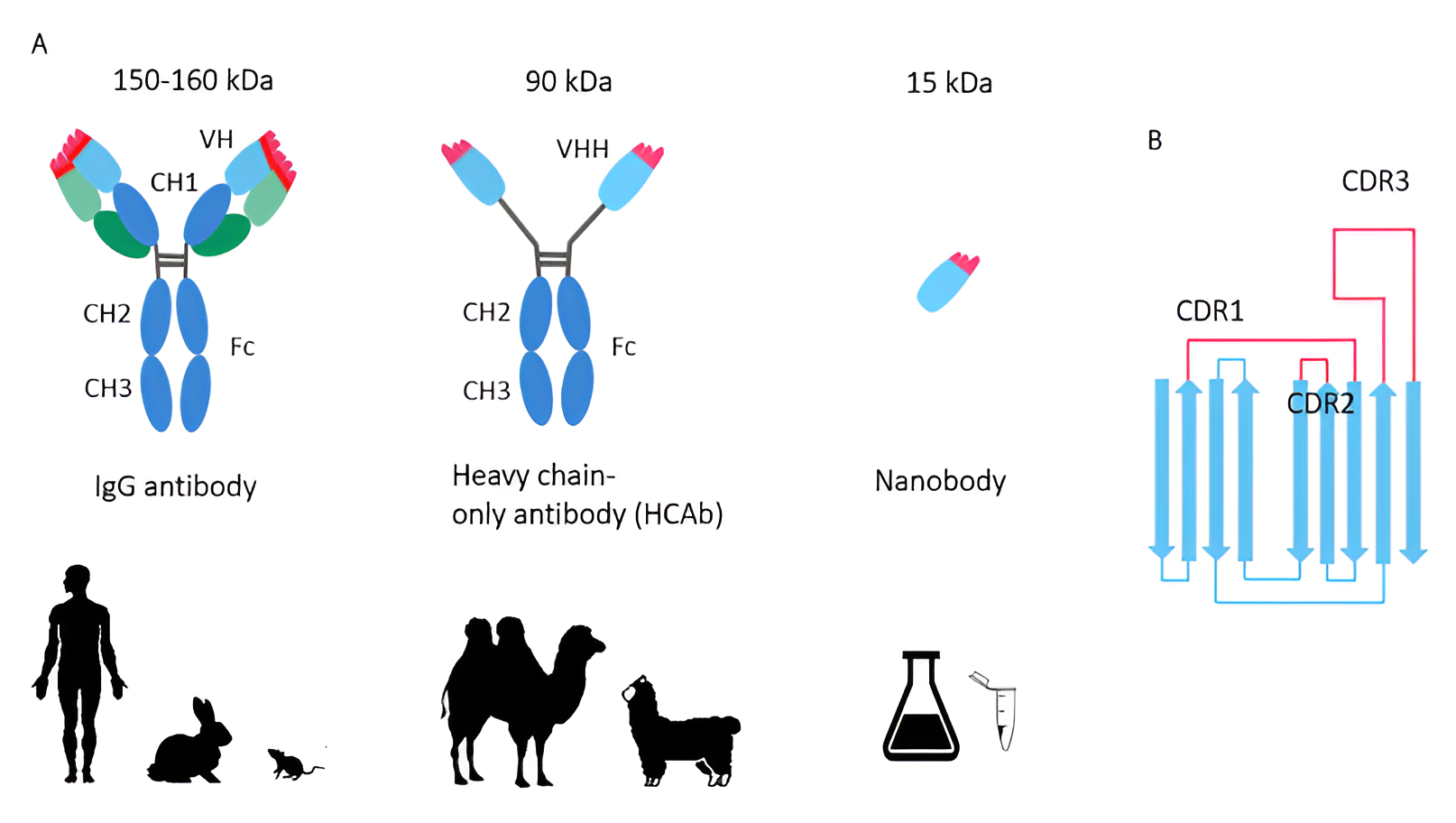
傳統抗體、僅含重鏈的抗體 (HCAbs) 與奈米抗體 (Nbs) (A) HCAb(圖中間)僅由兩條重鏈組成。其抗原結合部位稱做 VHH,為一條約 120 個胺基酸組成的單一鏈 (15 kDa)。(B) 奈米抗體的 CDR(互補決定位,紅色)與 FR(框架區,藍色)。CDR 對抗原的結合非常重要,通常比 IgG 的同源區域更長,使奈米抗體能接觸到難以到達的表位,例如:酶的催化位點。
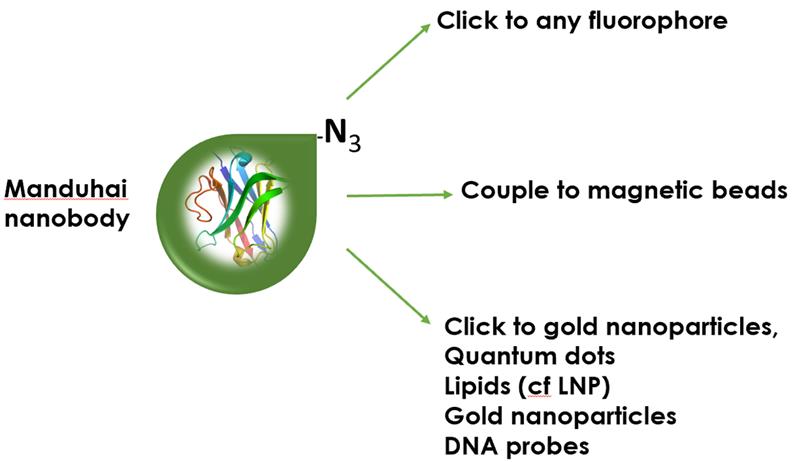
無論您從事的是基礎或應用(生物)醫學、動物或植物科學、藥理學、病毒學、微生物學、(超分辨率)顯微鏡學、疫苗研究或漁業科學,VHH 都能為您帶來前所未有的機會,揭示傳統基因技術或傳統抗體無法獲取的生物或臨床資訊。原因在於,蛋白質是所有生物體的基本組成元件,並以最根本的方式參與健康與疾病的發展。
遺傳方法往往會使目標蛋白質的所有功能遭到移除,並摧毀其整體互作網路。蛋白質通常與許多其他蛋白質形成交互作用,彼此建構出支撐各種細胞功能的互作網路。將 VHH/奈米抗體應用於您的研究,能使專案邁向新層次,並使您得以提出過去無法回答的新問題,進而以實驗方式加以探究。
VHHs 通常優於 IgGs 的關鍵應用範例
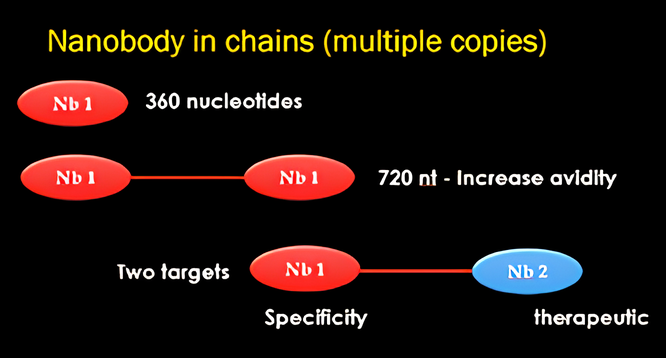


- 體積僅為 IgG 的十分之一。
- 擁有較長的 CDR 區,可在體內與體外有效阻斷酵素活性或干擾蛋白質間的互作。
- 是蛋白質體學研究的強大工具。
- 結構蛋白常缺乏有效抑制劑,奈米抗體正好填補此空缺。
- 能細緻地抑制蛋白功能,而非像 RNAi 一樣將目標蛋白質完全破壞。
- 更深入了解您的目標蛋白質的生物學特性。
- 奈米抗體在細胞質(還原性環境)中具高度穩定性。
- 奈米抗體 cDNA 皆可取得,隨時可用。
- 可避免 GFP 融合蛋白的過度表達,進而維持蛋白質體內平衡。
- 作為細胞內抗體使用時,可直接作用於內源性蛋白質。
- 高親和力結合劑(nanomolar 至 picomolar 等級)。
- 仍可對目標蛋白質進行成像(RNAi 無法達成)。
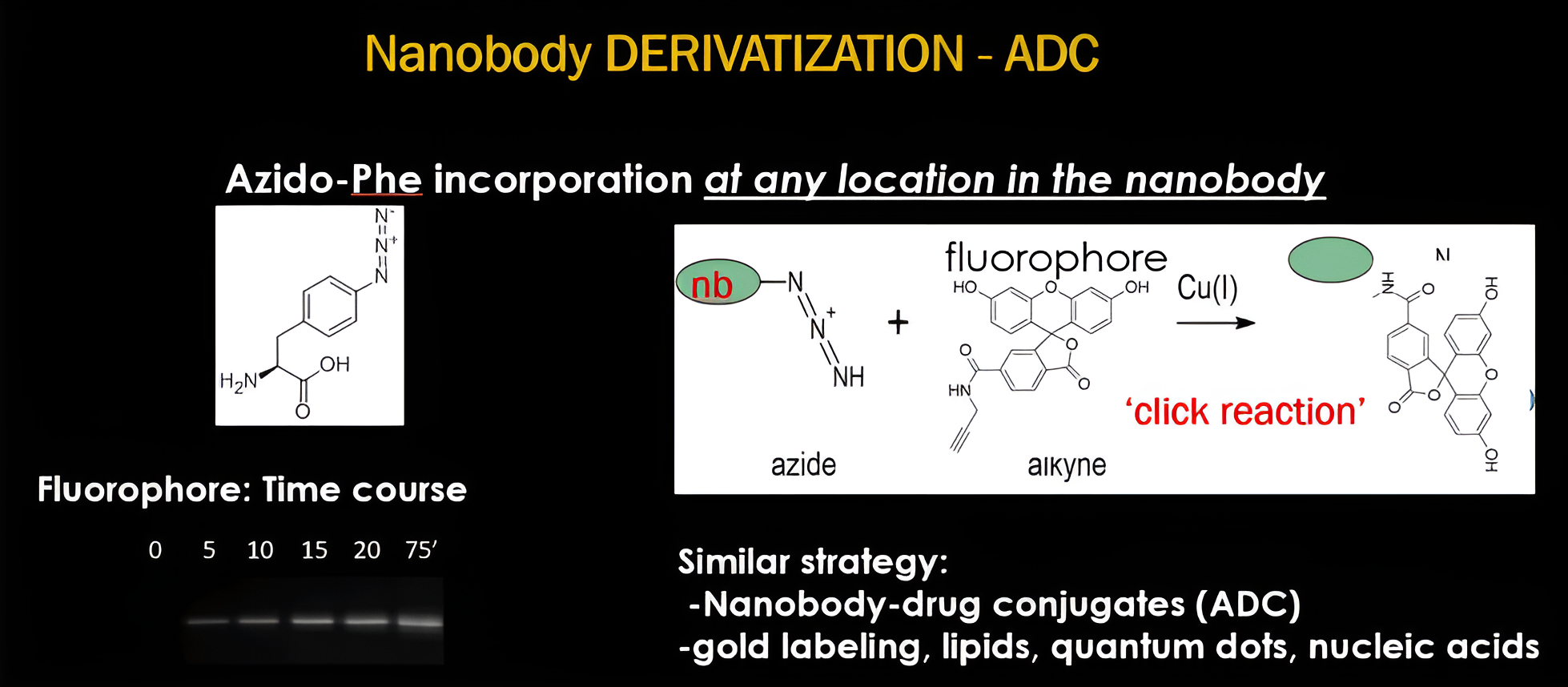
- 可在其一級結構中插入非天然胺基酸,實現位點特異性修飾。
- 可將螢光團特定位點耦聯至奈米抗體,實現極低連結誤差,適用於超解析顯微技術。
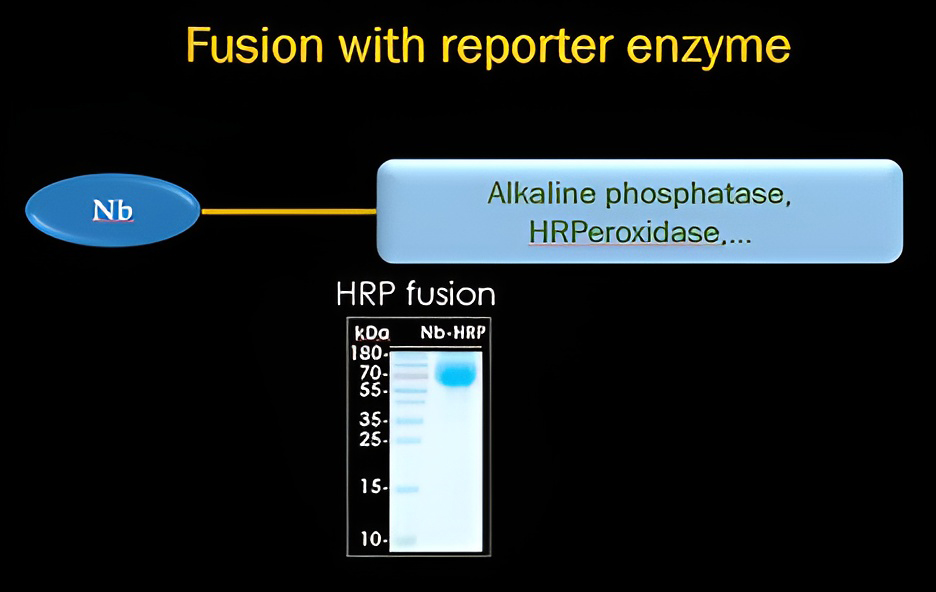
- 可將奈米抗體以共價方式連接至螢光團、磁珠、金奈米粒子、生物分子或藥物。
- 奈米抗體有助於蛋白質晶體化。
- 可識別目標蛋白質中的關鍵表位。
- 作為「不可藥物化」蛋白質的治療切入點。